Författare:
Carl Weaver
Skapelsedatum:
22 Februari 2021
Uppdatera Datum:
1 Juli 2024
Innehåll
- Steg
- Metod 1 av 2: Beräkna den molära absorptionskoefficienten med hjälp av formeln
- Metod 2 av 2: Grafisk upptäckt av den molära absorptionskoefficienten
- Ytterligare artiklar
Molarabsorptionskoefficienten, även känd som den molära extinktionskoefficienten, är ett mått på hur starkt kemiska partiklar (molekyler) av ett ämne absorberar ljus vid en specifik våglängd. Varje ämne kännetecknas av sin egen molära absorptionskoefficient, som är oberoende av koncentration och volym. Denna egenskap används i stor utsträckning inom kemi och bör inte förväxlas med utrotningskoefficienten, som är vanligare inom fysik. Standardmåttenheten för molar absorbans är liter dividerat med mol och per centimeter (L mol cm).
Steg
Metod 1 av 2: Beräkna den molära absorptionskoefficienten med hjälp av formeln
 1 Kolla in Bouguer-Lambert-Beer-lagen:A = ɛlc... Absorptionen av ljus i ett medium beskrivs av ekvationen A = ɛlc, var A - mängden ljus med en viss våglängd som absorberades av provet, ɛ - molär absorptionskoefficient, l är det avstånd som färdats av ljus i lösning, och c - lösningens koncentration (antalet studerade molekyler per volymenhet).
1 Kolla in Bouguer-Lambert-Beer-lagen:A = ɛlc... Absorptionen av ljus i ett medium beskrivs av ekvationen A = ɛlc, var A - mängden ljus med en viss våglängd som absorberades av provet, ɛ - molär absorptionskoefficient, l är det avstånd som färdats av ljus i lösning, och c - lösningens koncentration (antalet studerade molekyler per volymenhet). - Absorptionskoefficienten kan också hittas från förhållandet mellan intensiteten hos ljuset som överförs genom standarden och provet som undersöks. I detta fall är ekvationen enligt följande: A = logg10(Jago/ Jag).
- Ljusintensiteten bestäms med hjälp av en spektrofotometer.
- En lösnings absorptionskapacitet beror på våglängden för ljuset som passerar genom den. Vid vissa värden av våglängden absorberas ljuset starkare än vid andra, och dessa värden beror på lösningens sammansättning. Vid beräkning, glöm inte att ange för vilken våglängd de är gjorda.
 2 Konvertera Bouguer-Lambert-Beer-lagen för att uttrycka molär absorptionskoefficient. Dela ekvationen på båda sidor med längd och koncentration, och resultatet är ett uttryck för den molära absorptionskoefficienten: ɛ = A / lc... Med hjälp av denna formel kan du beräkna den molära absorptionskoefficienten för en specifik våglängd.
2 Konvertera Bouguer-Lambert-Beer-lagen för att uttrycka molär absorptionskoefficient. Dela ekvationen på båda sidor med längd och koncentration, och resultatet är ett uttryck för den molära absorptionskoefficienten: ɛ = A / lc... Med hjälp av denna formel kan du beräkna den molära absorptionskoefficienten för en specifik våglängd. - Absorptionskapaciteten vid ett fast avstånd beror på koncentrationen av lösningen och formen på den använda behållaren. Den molära absorptionskoefficienten eliminerar dessa faktorer.
 3 Mät de erforderliga värdena med hjälp av spektrofotometri. I en spektrofotometer passeras ljus med en specifik våglängd genom ett ämne och intensiteten hos det överförda ljuset mäts vid utgången. En del av ljuset absorberas av lösningen och ljusintensiteten minskar. Spektrofotometern mäter intensiteten hos det överförda ljuset, som används för att beräkna den molära absorptionskoefficienten.
3 Mät de erforderliga värdena med hjälp av spektrofotometri. I en spektrofotometer passeras ljus med en specifik våglängd genom ett ämne och intensiteten hos det överförda ljuset mäts vid utgången. En del av ljuset absorberas av lösningen och ljusintensiteten minskar. Spektrofotometern mäter intensiteten hos det överförda ljuset, som används för att beräkna den molära absorptionskoefficienten. - Förbered en lösning med känd koncentration för analys c... Bestäm koncentrationen i mol / gram eller mol / liter.
- För att bestämma l mäta kuvettens längd. Skriv ner längden i centimeter.
- Mät absorbansen med en spektrofotometer A för en specifik våglängd. Våglängd mäts i meter, men ljuset är så kort att det vanligtvis uttrycks i nanometer (nm). Absorptionskapaciteten är måttlös.
 4 Anslut siffrorna till ekvationen och hitta den molära absorptionskoefficienten. Ta numeriska värden A, c och l och anslut dem till formeln ɛ = A / lc... Multiplicera l på coch dela sedan A med denna mängd för att hitta den molära absorptionskoefficienten.
4 Anslut siffrorna till ekvationen och hitta den molära absorptionskoefficienten. Ta numeriska värden A, c och l och anslut dem till formeln ɛ = A / lc... Multiplicera l på coch dela sedan A med denna mängd för att hitta den molära absorptionskoefficienten. - Antag att du mätte absorbansen för en 0,05 mol / liter lösning med en 1 cm kyvett. I detta fall var absorbansen 1,5 för ljus med en våglängd på 280 nm. Hur hittar man den molära absorptionskoefficienten för en given lösning?
- ɛ280 = A / lc = 1,5 / (1 x 0,05) = 30 L mol cm
- Antag att du mätte absorbansen för en 0,05 mol / liter lösning med en 1 cm kyvett. I detta fall var absorbansen 1,5 för ljus med en våglängd på 280 nm. Hur hittar man den molära absorptionskoefficienten för en given lösning?
Metod 2 av 2: Grafisk upptäckt av den molära absorptionskoefficienten
 1 Mät intensiteten hos det överförda ljuset för olika koncentrationer av lösningen. Förbered 3-4 lösningar med olika koncentrationer.Använd en spektrofotometer för att mäta absorbansen av lösningar med olika koncentrationer för en given våglängd. Du kan börja med den lägsta koncentrationslösningen. Ordningen är inte viktig, det viktigaste är att inte förväxla och registrera de uppmätta absorbansvärdena i enlighet med koncentrationerna.
1 Mät intensiteten hos det överförda ljuset för olika koncentrationer av lösningen. Förbered 3-4 lösningar med olika koncentrationer.Använd en spektrofotometer för att mäta absorbansen av lösningar med olika koncentrationer för en given våglängd. Du kan börja med den lägsta koncentrationslösningen. Ordningen är inte viktig, det viktigaste är att inte förväxla och registrera de uppmätta absorbansvärdena i enlighet med koncentrationerna.  2 Plotta de erhållna värdena på diagrammet. Plotta koncentrationen på den horisontella X-axeln och absorbansen på den vertikala Y-axeln och rita upp mätningarna som prickar.
2 Plotta de erhållna värdena på diagrammet. Plotta koncentrationen på den horisontella X-axeln och absorbansen på den vertikala Y-axeln och rita upp mätningarna som prickar. - Dra en linje mellan punkterna. Om mätningarna utfördes korrekt bör punkterna ligga på en rak linje, eftersom absorptionskapaciteten enligt Bouguer-Lambert-Beer-lagen är direkt proportionell mot koncentrationen.
 3 Definiera lutning raktpasserar genom de experimentella punkterna. För att hitta lutningen för en rak linje, dividera Y -ökningen med X -abscissastegningen. Ta två punkter på linjen, subtrahera motsvarande koordinater för en punkt från koordinaterna för den andra och dela Y -skillnaden med X -skillnaden.
3 Definiera lutning raktpasserar genom de experimentella punkterna. För att hitta lutningen för en rak linje, dividera Y -ökningen med X -abscissastegningen. Ta två punkter på linjen, subtrahera motsvarande koordinater för en punkt från koordinaterna för den andra och dela Y -skillnaden med X -skillnaden. - Lutningen för en rak linje (lutningen eller tangenten för lutningen) finns enligt följande: (Y2 - Y1) / (X2 - X1). I detta fall tilldelas den punkt som ligger högre längs den raka linjen index 2 och den nedre punkten - indexet 1.
- Antag att vid en molkoncentration av 0,2 var absorbansen 0,27, och vid en koncentration av 0,3 var den 0,41. Absorbans ritas på Y-axeln och koncentration på X-axeln. Använd ovanstående ekvation för att hitta lutningen för en rak linje: (Y2 - Y1) / (X2 - X1) = (0,41-0,27)/(0,3-0,2) = 0,14/0,1 = 1,4.
 4 För att hitta den molära absorptionskoefficienten, dividera lutningen på en rak linje med den väg som ljuset färdades (kyvettens djup). Banans färd med ljuset är lika med djupet på kyvetten som används i spektrofotometern.
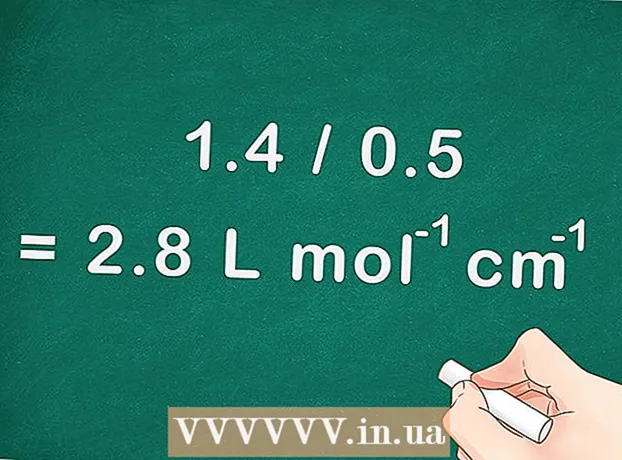
4 För att hitta den molära absorptionskoefficienten, dividera lutningen på en rak linje med den väg som ljuset färdades (kyvettens djup). Banans färd med ljuset är lika med djupet på kyvetten som används i spektrofotometern. - För vårt exempel får vi: om lutningen är 1,4 och kyvettens djup är 0,5 centimeter, då är den molära absorptionskoefficienten 1,4 / 0,5 = 2,8 L mol cm.
Ytterligare artiklar
 Hur man beräknar kvadratmeter
Hur man beräknar kvadratmeter  Hur man hittar antalet protoner, neutroner och elektroner
Hur man hittar antalet protoner, neutroner och elektroner  Hur man bestämmer valenselektroner
Hur man bestämmer valenselektroner  Hur man balanserar kemiska ekvationer
Hur man balanserar kemiska ekvationer  Hur man skriver den elektroniska konfigurationen av en atom av något element
Hur man skriver den elektroniska konfigurationen av en atom av något element  Hur man beräknar koncentrationen av en lösning
Hur man beräknar koncentrationen av en lösning  Hur man beräknar molariteten i en lösning
Hur man beräknar molariteten i en lösning  Hur man hittar antalet neutroner i en atom
Hur man hittar antalet neutroner i en atom  Hur man gör dricksvatten från salt
Hur man gör dricksvatten från salt  Hur man använder det periodiska systemet
Hur man använder det periodiska systemet  Hur man förvarar torris
Hur man förvarar torris  Hur man gör torris
Hur man gör torris  Hur man gör elefant tandkräm
Hur man gör elefant tandkräm  Hur man spädar lösningen
Hur man spädar lösningen