Författare:
Bobbie Johnson
Skapelsedatum:
10 April 2021
Uppdatera Datum:
1 Juli 2024
Innehåll
Vattenklyvningsprocess (H2O) i dess beståndsdelar (väte och syre) som använder elektricitet kallas elektrolys. De gaser som erhålls som ett resultat av elektrolys kan användas på egen hand - till exempel fungerar väte som en av de renaste energikällorna. Även om namnet på denna process kan låta lite smart, är det faktiskt enklare än det kan tyckas om du har rätt utrustning, kunskap och lite erfarenhet.
Steg
Del 1 av 2: Förbered utrustningen
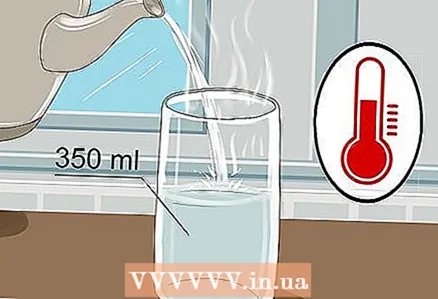 1 Ta ett 350 ml glas och häll varmt vatten i det. Det finns ingen anledning att fylla glaset till brädden, bara lite vatten räcker. Kallt vatten klarar sig, även om varmt vatten leder elektricitet bättre.
1 Ta ett 350 ml glas och häll varmt vatten i det. Det finns ingen anledning att fylla glaset till brädden, bara lite vatten räcker. Kallt vatten klarar sig, även om varmt vatten leder elektricitet bättre. - Både kranvatten och flaskvatten kommer att göra.
- Varmt vatten har en lägre viskositet, vilket gör det lättare för joner att röra sig.
 2 Lös upp 1 matsked (20 gram) bordsalt i vatten. Häll salt i ett glas och rör om vattnet för att lösa upp. Detta skapar en saltlösning.
2 Lös upp 1 matsked (20 gram) bordsalt i vatten. Häll salt i ett glas och rör om vattnet för att lösa upp. Detta skapar en saltlösning. - Natriumklorid (dvs bordsalt) är en elektrolyt som ökar vattnets elektriska konduktivitet. I sig leder vatten inte bra el.
- När du har ökat vattnets elektriska ledningsförmåga kommer strömmen som skapas av batteriet lättare att passera genom lösningen och mer effektivt bryta ner molekylerna till väte och syre.
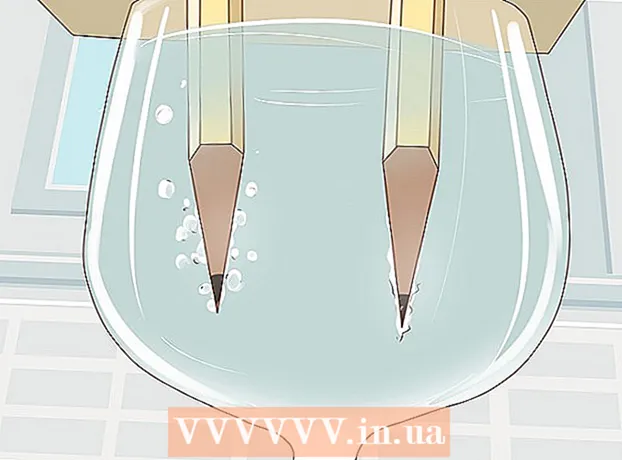
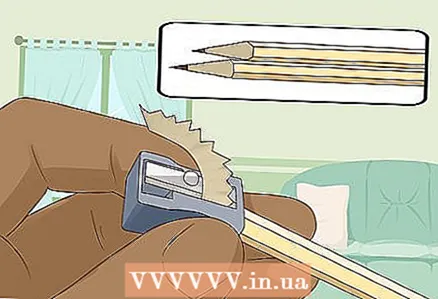 3 Slipa två hårt mjuka pennor i båda ändarna för att avslöja ledningen. Glöm inte att ta bort suddgummit från dina pennor. En grafitstav bör sticka ut i båda ändarna.
3 Slipa två hårt mjuka pennor i båda ändarna för att avslöja ledningen. Glöm inte att ta bort suddgummit från dina pennor. En grafitstav bör sticka ut i båda ändarna. - Grafitstavarna fungerar som isolerade elektroder som du ansluter batteriet till.
- Grafit är väl lämpad för detta experiment eftersom det inte löser sig eller korroderar i vatten.
 4 Klipp ut en kartong som är tillräckligt stor för att ligga ovanpå glaset. Använd en ganska tjock kartongbit som inte hänger efter att du har slagit två hål i den. Skär en fyrkantig bit ur en skokartong eller liknande.
4 Klipp ut en kartong som är tillräckligt stor för att ligga ovanpå glaset. Använd en ganska tjock kartongbit som inte hänger efter att du har slagit två hål i den. Skär en fyrkantig bit ur en skokartong eller liknande. - Kartongen används för att hålla pennorna i vattnet så att de inte vidrör sidorna och botten av glaset.
- Kartong är icke-ledande, så du kan säkert lägga den på ett glas.
 5 Använd pennor för att sticka två hål i kartongen. Hål i kartongen med pennor - i detta fall kommer de att klämmas tätt och glida inte. Se till att grafiten inte vidrör sidorna eller botten av glaset, annars kommer det att störa experimentet.
5 Använd pennor för att sticka två hål i kartongen. Hål i kartongen med pennor - i detta fall kommer de att klämmas tätt och glida inte. Se till att grafiten inte vidrör sidorna eller botten av glaset, annars kommer det att störa experimentet.
Del 2 av 2: Gör ett experiment
 1 Anslut en tråd med krokodilklämmor till varje batteripol. Batteriet kommer att fungera som en källa till elektrisk ström, och genom ledningarna med klämmor och grafitstavar kommer strömmen att nå vattnet.Anslut en tråd med en klämma till pluspolen och den andra till batteriets minuspol.
1 Anslut en tråd med krokodilklämmor till varje batteripol. Batteriet kommer att fungera som en källa till elektrisk ström, och genom ledningarna med klämmor och grafitstavar kommer strömmen att nå vattnet.Anslut en tråd med en klämma till pluspolen och den andra till batteriets minuspol. - Använd ett 6 volts batteri. Om du inte har ett kan du istället använda ett 9-voltsbatteri.
- Ett lämpligt batteri kan fås från en elförsörjningsbutik eller stormarknad.
 2 Anslut trådarnas andra ändar till pennorna. Fäst metalltrådsklämmorna ordentligt på grafitstavarna. Du kan behöva skala av lite mer trä från pennorna för att klipparna inte ska glida av grafitstavarna.
2 Anslut trådarnas andra ändar till pennorna. Fäst metalltrådsklämmorna ordentligt på grafitstavarna. Du kan behöva skala av lite mer trä från pennorna för att klipparna inte ska glida av grafitstavarna. - Således stänger du kretsen och ström från batteriet kommer att flöda genom vattnet.
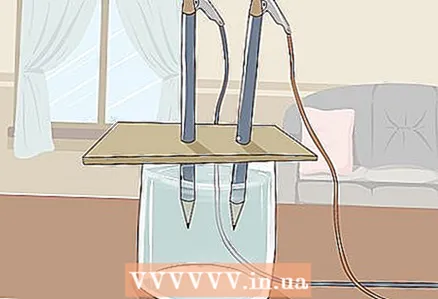 3 Lägg kartongen på glaset så att pennornas fria ändar är nedsänkta i vattnet. Kartongen ska vara tillräckligt stor för att vila på glaset. Var försiktig så att du inte stör den korrekta placeringen av pennorna.
3 Lägg kartongen på glaset så att pennornas fria ändar är nedsänkta i vattnet. Kartongen ska vara tillräckligt stor för att vila på glaset. Var försiktig så att du inte stör den korrekta placeringen av pennorna. - För att experimentet ska lyckas får grafiten inte vidröra glasets väggar och botten. Kontrollera detta igen och justera pennorna vid behov.
 4 Se vattnet delas upp i väte och syre. Gasbubblor kommer att börja stiga från grafitstavarna nedsänkta i vattnet. Dessa är väte och syre. Väte kommer att frigöras vid den negativa polen och syre vid den positiva polen.
4 Se vattnet delas upp i väte och syre. Gasbubblor kommer att börja stiga från grafitstavarna nedsänkta i vattnet. Dessa är väte och syre. Väte kommer att frigöras vid den negativa polen och syre vid den positiva polen. - Så snart du ansluter ledningarna till batteriet och grafitstavarna kommer en elektrisk ström att flöda genom vattnet.
- Fler gasbubblor kommer att bildas på pennan som är ansluten till den negativa polen, eftersom varje vattenmolekyl består av två väteatomer och en syreatom.
Tips
- Om du inte har pennor med grafitskaft kan du istället använda två små trådar. Vik bara ena änden av varje tråd runt motsvarande batteripol och doppa den andra i vattnet. Resultatet blir detsamma som med pennor.
- Prova att använda ett annat batteri. Mängden ström som flödar beror på batteriets spänning, vilket i sin tur påverkar splittringen av vattenmolekyler.
Varningar
- Om du lägger till en elektrolyt, till exempel salt, i vattnet, kom ihåg att experimentet kommer att generera en liten mängd av en biprodukt som klor. Det är säkert i så små mängder, men du kan känna en liten klorlukt.
- Utför detta experiment under övervakning av vuxna. Det är associerat med el och gaser och kan därför vara farligt, men osannolikt.
Vad behöver du
- Två hårda mjuka pennor
- Ett 6 eller 9 volt batteri
- Glas med en volym på 350 milliliter
- 2 trådar med krokodilklämmor
- Slipmedel för penna
- Salt