Författare:
Louise Ward
Skapelsedatum:
11 Februari 2021
Uppdatera Datum:
1 Juli 2024

Innehåll
Storleken på en atom är så liten att det är svårt att noggrant mäta atomnummer för en kemisk förening. För att kunna mäta en mängd ämnen exakt använder forskare en molenhet för att representera ett specificerat antal atomer. En mol substans definieras som ekvivalent med antalet kolatomer som finns i 12 gram av 12 kolisotopen, vilket är cirka 6 022 x 10 atomer. Detta värde kallas Avogadro-numret eller Avogadro-konstanten. Detta kallas också antalet atomer i 1 mol av något element, och 1 mol av massan av ett ämne kallas molmassan för det ämnet.
Steg
Metod 1 av 2: Beräkna molmassan för ett element
Definition av molär massa. Molmassa för ett ämne är massan (i gram) av en mol av ämnet. För att beräkna molmassan för ett element, multiplicera dess atommassa med gram-per-mol-omvandlingsfaktorn (g / mol).
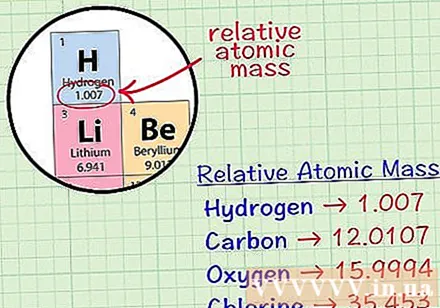
Hitta den genomsnittliga kubiska atomen för ett element. Den genomsnittliga massatomen för ett element är den genomsnittliga massan, i atomenheter, i ett prov som innehåller alla isotoper av det elementet. Denna information ges ofta i det periodiska elementet. Genom att hitta ett element kan du hitta en genomsnittlig kubisk atom skriven strax under elementets kemiska symbol. Detta värde är inte ett heltal utan ett tal med decimaler.- Till exempel, med väte är den genomsnittliga massatomen 1,007; Den genomsnittliga kubikatomen av kol är 12 0107; Den genomsnittliga massatomen för syre är 15 9994; klor har en genomsnittlig atommassa på 35 453.

Multiplicera den genomsnittliga massatomen med molmassakonstanten. Enheten för molglid definieras som 0,001 kg per mol eller 1 gram per mol. Produkten av den genomsnittliga massatomen och molmassakonstanten omvandlar enheten med atommassa till gram per mol, så den molära massan av väte blir 1,007 gram per mol, kol är 12. 0107 gram per mol, syre är 15 9995 gram per mol och klor är 35 453 gram per mol.- Vissa element finns i naturen som molekyler som består av två eller flera av samma atomer. Det vill säga om du vill beräkna molmassan av föreningar som består av mer än en atom, såsom vätgas, syrgas eller klorgas, måste du bestämma föreningens genomsnittliga atommassa och multiplicera detta värde. med den molära massan konstant, '' sedan '' multiplicerar du produkten du just hittade med 2.
- Med H2: 1 007 x 2 = 2 014 gram per mol; för O2: 15,9994 x 2 = 31,9988 gram per mol; och Cl2: 35 453 x 2 = 70 096 gram per mol.
Metod 2 av 2: Beräkna molmassan för föreningen

Bestäm strukturformeln för föreningen. En substans strukturformel ger atomnumret för varje element som utgör den föreningen. (Denna information finns i alla referensböcker). Till exempel är den kemiska formeln för saltsyra HCl; av glukos är C6H12O6. Med denna strukturformel kan vi bestämma antalet för varje typ av atom som utgör föreningen som övervägs.- Där HCl har en väteatom och en kloratom.
- Glukossockermolekyl C6H12O6 har 6 kolatomer, 12 väteatomer och 6 syreatomer.
Bestäm den genomsnittliga massatomen för varje beståndsdel. Använd det periodiska systemet för att hitta den genomsnittliga massatomen för varje element som finns i föreningen. Den genomsnittliga massatomen skrivs vanligtvis under elementets kemiska symbol på det periodiska systemet. På samma sätt som att beräkna molmassan för ett element multiplicerar du den genomsnittliga massatomen med 1 gram / mol.
- Den genomsnittliga massatomen för elementen som bildar saltsyra är som följer: väte 1,007 g / mol och klor 35,453 g / mol.
- Den genomsnittliga massatomen för elementen som utgör glukosmolekylen är: kol, 12 017 g / mol; väte, 1007 g / mol; och syre, 15,9995 g / mol.
Beräkna molmassan för varje komponentelement. Att multiplicera ett grunds massa atom med antalet atomer som det bidrar i en förening ger den genomsnittliga massan av elementet i föreningen.
- När det gäller saltsyra, HCl, är molmassan för grundämnet väte 1 007 g / mol och den för klor är 35 453 g / mol.
- När det gäller glukos, C6H12O6, molmassan för varje element är som följer: kol, 12,0107 x 6 = 72 06642 g / mol; väte, 1007 x 12 = 12 084 g / mol; syre, 15,9995 x 6 = 95,9964 g / mol.
Total molmassa för beståndsdelarna. Komposteringselementens totala molmassa är föreningens molmassa.I föregående steg beräknade vi molmassan för varje element som finns i föreningen, i detta steg behöver vi bara lägga till alla dessa värden.
- Molmassa av saltsyra är 1 007 + 35 453 = 36 460 g / mol. 36,46 gram är massan av 1 mol saltsyra.
- Molmassa av glukos är 72 0664 + 12 084 + 95 9964 = 180 1446 g / mol. Så varje mol glukos har en massa på 180,14 gram.
Råd
- Även om den genomsnittliga massatomen i de flesta fall registreras till närmaste 1 del 1000 (4 decimaler), reduceras molmassan i laboratorier ofta till 2 decimaler, ibland ännu mindre för stora molekyler. I laboratoriefallen kan därför molmassan av saltsyra skrivas till 36,46 gram per mol, för glukos 180,14 gram per mol.
Vad du behöver
- Kemisk referensbok eller periodiskt element
- Dator



